易倍新闻 

2024年7月27日-28日,“2024乳腺癌夏季论坛·北方沙龙”在北京顺利召开,秉承“学习吸收、创新提高”的理念,乳腺癌领域专家齐聚一堂,深入探讨乳腺癌领域最新研究进展与前沿诊疗理念。近年来,免疫治疗在三阴性乳腺癌(TNBC)领域崭露头角,我国原研PD-1单抗特瑞普利单抗更是实现了国内晚期TNBC领域免疫治疗零的突破,为患者带来了新的治疗希望,并在世界舞台彰显了中国力量与中国智慧。值此之际,医脉通特邀围绕特瑞普利单抗在中国获批晚期TNBC一线治疗适应证及TNBC免疫治疗等相关话题分享真知灼见。
医脉通:作为乳腺癌免疫治疗的优势亚型,TNBC具有较高的肿瘤免疫原性,免疫治疗在TNBC领域的重要性愈加凸显。请您结合相关诊疗指南及专家共识,分享目前免疫治疗在晚期TNBC中有着怎样的治疗地位和价值?
临床对于TNBC比较关注,主要原因在于与HR阳性乳腺癌和HER2阳性乳腺癌相比,TNBC缺乏针对性治疗手段,治疗方式较少,晚期患者整体生存时间较短,如HR阳性乳腺癌患者的5年生存率可以达到50%,而TNBC患者的5年生存率仅有12%左右。既往TNBC治疗以化疗为主,传统化疗药物紫衫类联合吉西他滨或卡倍他滨治疗晚期TNBC,无进展生存期(PFS)仅6个月左右,后续紫衫类联合铂类化疗药物将晚期TNBC患者的PFS提升至7或8个月,但患者总生存期(OS)一般为一年多,整体生存获益有限,晚期TNBC传统化疗疗效达到了瓶颈。免疫治疗作为肿瘤研究的热点,在其它瘤种中已经显示出了较好的疗效,其在乳腺癌领域的应用也是临床探索的重点方向,TNBC是一种免疫原性较高的乳腺癌亚型,患者肿瘤突变负荷(TMB)、PD-L1表达以及肿瘤浸润淋巴细胞(TIL)水平较高,提示TNBC有望从免疫治疗中获益。
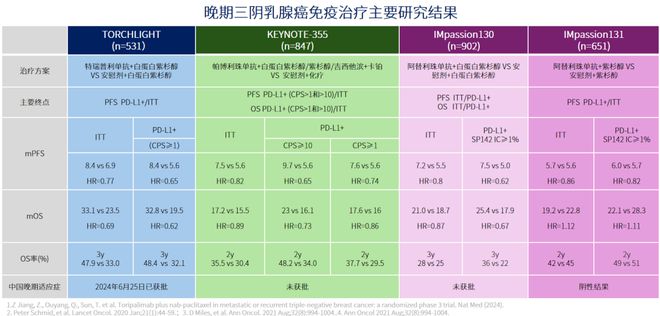
基于此,临床开展了PD-1/PD-L1抑制剂治疗TNBC的临床研究。但免疫检查点抑制剂单药治疗晚期TNBC的获益较为局限,有效率不到20%。从作用机理而言,免疫治疗联合化疗具有正向调节作用,化疗能够引起细胞死亡,促进抗原释放,从而正向促进免疫治疗疗效,因此免疫治疗联合化疗方案成为晚期TNBC治疗的研究重点,且展现出了较好疗效。国外KEYNOTE-355研究结果显示[1,2],与单独化疗相比,帕博利珠单抗联合化疗治疗晚期TNBC显著改善了PD-L1阳性(CPS≥10)患者PFS和OS(23.0个月 vs 16.1个月;HR=0.73,95%CI 0.55-0.95;P=0.0185),但对于CPS≥1亚组患者,OS并未达显著获益(17.6个月 vs 16.0个月;P=0.1125)。
而君实生物自主研发的PD-1抑制剂特瑞普利单抗布局晚期TNBC领域开展的TORCHLIGHT研究证实[3],与单独化疗相比,特瑞普利单抗联合白蛋白结合型紫杉醇一线治疗晚期TNBC能够显著改善PD-L1阳性(CPS≥1)患者的PFS(8.4个月 vs 5.6个月;HR=0.65,95%CI 0.470-0.906;P=0.0102)和OS(32.8个月 vs 19.5个月,HR=0.62,95%CI 0.414-0.914,P=0.0148)。基于TORCHLIGHT研究的突破性结果,国家药品监督管理局(NMPA)批准了特瑞普利单抗联合注射用紫杉醇(白蛋白结合型)用于经充分验证的检测评估PD-L1阳性(CPS≥1)的复发或转移性TNBC的一线版 CSCO 乳腺癌诊疗指南[4]也将特瑞普利单抗联合白蛋白结合型紫杉醇列为晚期TNBC(紫杉醇敏感)患者解救化疗+免疫治疗的I级推荐(1A类证据)。特瑞普利单抗为中国TNBC临床带来了更好的治疗选择,也为TNBC患者带来了更好的临床疗效。
医脉通:不同免疫联合方案在TNBC临床研究中具体不同的表现。请您结合相关研究进展,分享目前关于TNBC免疫联合策略的探索,并剖析特瑞普利单抗与白蛋白紫杉醇为何可实现“1+1>2”?
PD-1/PD-L1抑制剂在TNBC领域的临床研究有成功也有失败,不同免疫联合治疗方案具有不同的表现,如探究阿替利珠单抗联合白蛋白结合型紫杉醇治疗晚期TNBC的IMpassion130研究[5]仅取得了PFS获益,OS未达显著获益。随后的IMpassion131研究[6]将白蛋白紫杉醇更换为紫杉醇,结果显示ITT人群与PD-L1阳性人群的PFS和OS均未得到改善,基于这一阴性结局,阿替利珠单抗在晚期TNBC的适应证被撤回。而在TORCHLIGHT研究中,特瑞普利单抗联合白蛋白结合型紫杉醇实现了1+1>2的治疗效果,在CPS≥1患者中,这一联合方案取得了令人惊喜的治疗获益,患者OS可达32.8个月。而在KEYNOTE-355研究中,帕博利珠单抗联合化疗(白蛋白紫杉醇、紫杉醇或吉西他滨联合卡铂)仅改善了CPS≥10的生存,对于CPS≥1亚组患者,OS并未达显著获益(17.6个月 vs 16.0个月;P=0.1125)。由此可见,对于晚期TNBC患者,免疫联合化疗方案的疗效不仅与联合的化疗药物具有一定相关性,更与免疫治疗药物本身特性密切相关。
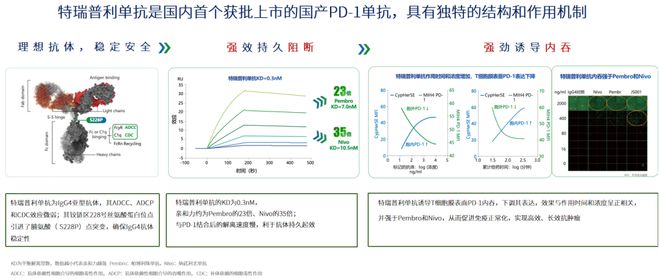
特瑞普利单抗具有“强效阻断”与“强效内吞”的特殊作用机制,与PD-1具有更强的亲和力,可阻断PD-1/PD-L1通路,提高抗肿瘤疗效,并且能够强力介导PD-1内吞,降低PD-1膜表面表达,无论PD-L1如何动态变化,PD-1内吞使PD-L1/PD-1通路均能被阻断,使肿瘤持久缓解。基于这一特殊作用机制,特瑞普利单抗联合白蛋白结合型紫杉醇实现了1+12的卓越疗效,打破了国内晚期TNBC免疫治疗无药可用的窘境,也为更广泛TNBC人群带来了免疫治疗的希望。
此外,值得一提的是,IMpassion130研究与KEYNOTE-355研究中纳入的亚洲患者均只占全部患者的20%左右,而特瑞普利单抗作为国产PD-1抑制剂,其关键性临床研究TORCHLIGHT入组的患者全部为中国患者,因此,特瑞普利单抗联合白蛋白结合型紫杉醇这一方案取得的治疗获益对于中国晚期TNBC人群而言更具代表性。
医脉通:可以发现,在不同的临床研究中,应用的PD-L1检测方式存在差异,免疫治疗的获益人群也有所不同。请您谈谈PD-L1检测对于识别乳腺癌免疫治疗获益人群的意义和价值。以及作为伴随诊断,PD-L1检测目前还有哪些需要改进的方向?
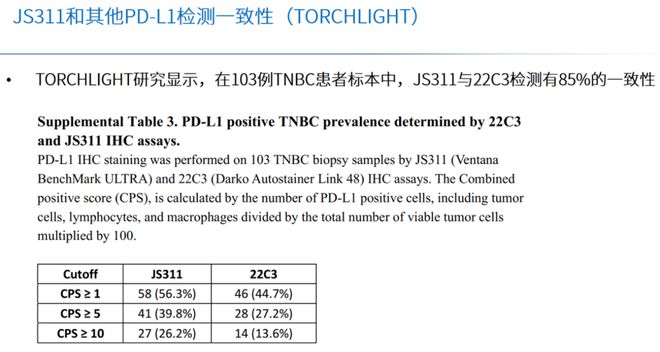
晚期乳腺癌患者PD-L1表达水平与PD-1/PD-L1抑制剂疗效相关,因此PD-L1检测对于识别乳腺癌免疫治疗潜在获益患者至关重要。KEYNOTE-355研究与TORCHLIGHT研究均证实了免疫治疗联合化疗治疗PD-L1阳性人群的获益,但两个研究定义的PD-L1阳性人群有所不同,并且选择的PD-L1检测抗体也不同。KEYNOTE-355研究采用22C3抗体进行PD-L1检测,PD-L1阳性人群定义为CPS≥10。而TORCHLIGHT研究采用JS311抗体,PD-L1阳性人群定义为CPS≥1。一项交叉相关研究使用了103例TNBC患者的肿瘤活检样本,比较了JS311和22C3抗体检测PD-L1的一致性,结果发现22C3和JS311在不同CPS截止点的总体一致性可以超过85%[3],提示不同PD-L1检测方式的结果具有一致性,均可以指导TNBC患者免疫治疗用药,并从侧面佐证了TORCHLIGHT研究扩大了TNBC免疫治疗获益人群。
2024乳腺癌免疫治疗临床应用专家共识[7]建议优先在石蜡包埋组织中进行PD-L1检测,手术切除标本和活检标本均可用于PD-L1检测(IA,1级),原发性和复发/转移病灶均可用于PD-LI检测,建议优先在复发转移病灶(IA,2级)的肿瘤组织中进行检测。但TNBC异质性较强,不同区域穿刺标本之间以及原发灶和转移灶的PD-L1表达存在一定的时间异质性与空间异质性,对于PD-L1检测结果存在一定影响。

[4]中国临床肿瘤学会指南工作委员会. CSCO乳腺癌诊疗指南2024.
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。













